QUÍMICA ORGÂNICA III
A solubilidade das substâncias e o seu comportamento em um processo de purificação dependem da sua natureza química. As funções orgânicas presentes em uma estrutura química determinam, em muitos casos, as propriedades ácido-base da substância em questão. Analisando os compostos: ácido propanoico, ácido cloro-etanoico, ácido 2,2 dicloro-propanoico, ácido etanoico e ácido 2-cloro-propanoico, qual das duas substâncias possui maior caráter ácido?
Ácido 2-cloro-propanoico
Ácido etanoico
Ácido 2,2 dicloro-propanoico
Ácido propanoico
Ácido cloro-etanoico
Considerando que um determinado composto orgânico, dissolvido em 100 mL de uma solução aquosa, foi submetido a uma extração líquido-líquido utilizando 200 mL de tolueno. Sabe-se que a razão de distribuição para o analito é de 1/90. Considerando que, na fase aquosa, há 20 g do composto orgânico, calcule o peso da amostra que passa para a fase orgânica num processo realizado em duas etapas, casa uma utilizando 100 mL de fase orgânica.
10 g
2,46 x 10-7 g
19,999 g
5 g
0,218 g
Podemos definir destilação como sendo uma operação que consiste na separação de substâncias químicas de suas eventuais misturas, baseado em suas diferenças de volatilidade. O processo de destilação é classificado como uma:
Operação unitária ou um processo de separação química, portanto ocorre reação química.
Operação unitária ou um processo de separação física, portanto não ocorre reação química.
Operação binária ocorrendo reação química.
Operação binária, não ocorrendo reação química.
Operação unitária, ou processo de separação físico-química, portanto ocorre reação química.
O controle de pulgas em animais de estimação pode ser feito utilizando-se a droga lufenurona, cuja estrutura química está representada abaixo.
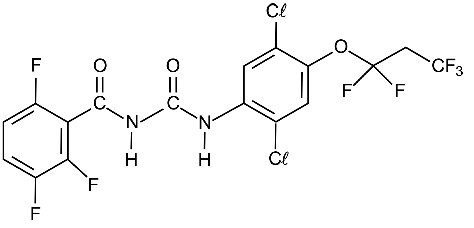 A lufenurona interfere na produção de quitina, componente que forma o exoesqueleto da pulga, levando o parasita à morte. A lufenurona possui:
A lufenurona interfere na produção de quitina, componente que forma o exoesqueleto da pulga, levando o parasita à morte. A lufenurona possui:
Um carbono assimétrico.
Seis ligações covalentes π.
A função amina.
Doze átomos de carbono com hibridização sp2.
Fórmula molecular C17H8O3N2F8Cl2.
Observe as moléculas abaixo.
I) CH3CH2CH2OH
II) CH3-CHOH-CH3
III) CH3-O-CH2-CH3
Assinale a alternativa correta.
As moléculas I e II são isômeros de posição e I e III são isômeros de função.
As moléculas I e II são isômeros de cadeia e II e III são isômeros de função.
As moléculas II e III não são isômeros.
As moléculas I e III são isômeros de cadeia, assim como as moléculas II e III.
As moléculas I e III são isômeros de posição.
A equação a seguir representa a reação entre o benzeno e o cloreto de etanoíla, onde se utilizou cloreto de alumínio como catalisador. Verifique qual o tipo de reação está sendo exemplificado:
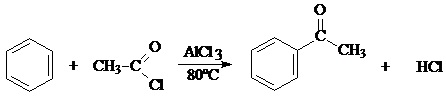
Nitração
Acilação
Sulfonação
Cloração
Alquilação
Um determinado composto orgânico dissolvido em 50 mL de uma solução foi submetido a duas extrações líquido-líquido utilizando 10 mL de octanol. Sabe-se que a razão de distribuição para o analito é de 1/70. Considerando que, na fase aquosa, há 1,58 g do composto orgânico. Qual a massa do analito que foi extraído?
1,575 g
0,796 g
0,582 g
1,010 g
1,580 g
Um composto orgânico com características básicas pode ser removido de sua solução em um solvente orgânico, pelo tratamento com uma solução ácida. Analisando o composto abaixo, é correto afirmar que:
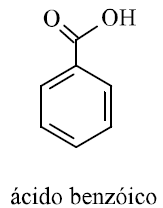
Possui caráter básico.
Seu respectivo sal é solúvel em água.
É um composto insolúvel em diclorometano.
Seu respectivo sal é solúvel em diclorometano.
É um composto solúvel em água.
Analisando as estruturas químicas, a seguir, explique por que o sal do ácido benzóico (benzoato de sódio) é mais solúvel em água do que o ácido benzóico.
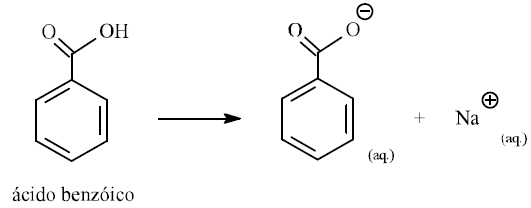
O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.
O coeficiente de distribuição ou partição (Kd) é uma constante de equilíbrio que descreve a distribuição do soluto entre duas fases imiscíveis. Logo, para um soluto A, o coeficiente de partição, Kd, entre ligroína e água é 7,5. Que massa de A seria removida de uma solução de 10 g de A em 100 mL de água, por uma única extração com 100 mL de ligroína?
Ácido 2-cloro-propanoico
Ácido etanoico
Ácido 2,2 dicloro-propanoico
Ácido propanoico
Ácido cloro-etanoico
Considerando que um determinado composto orgânico, dissolvido em 100 mL de uma solução aquosa, foi submetido a uma extração líquido-líquido utilizando 200 mL de tolueno. Sabe-se que a razão de distribuição para o analito é de 1/90. Considerando que, na fase aquosa, há 20 g do composto orgânico, calcule o peso da amostra que passa para a fase orgânica num processo realizado em duas etapas, casa uma utilizando 100 mL de fase orgânica.
10 g
2,46 x 10-7 g
19,999 g
5 g
0,218 g
Podemos definir destilação como sendo uma operação que consiste na separação de substâncias químicas de suas eventuais misturas, baseado em suas diferenças de volatilidade. O processo de destilação é classificado como uma:
Operação unitária ou um processo de separação química, portanto ocorre reação química.
Operação unitária ou um processo de separação física, portanto não ocorre reação química.
Operação binária ocorrendo reação química.
Operação binária, não ocorrendo reação química.
Operação unitária, ou processo de separação físico-química, portanto ocorre reação química.
O controle de pulgas em animais de estimação pode ser feito utilizando-se a droga lufenurona, cuja estrutura química está representada abaixo.
 A lufenurona interfere na produção de quitina, componente que forma o exoesqueleto da pulga, levando o parasita à morte. A lufenurona possui:
A lufenurona interfere na produção de quitina, componente que forma o exoesqueleto da pulga, levando o parasita à morte. A lufenurona possui:
Um carbono assimétrico.
Seis ligações covalentes π.
A função amina.
Doze átomos de carbono com hibridização sp2.
Fórmula molecular C17H8O3N2F8Cl2.
Observe as moléculas abaixo.
I) CH3CH2CH2OH
II) CH3-CHOH-CH3
III) CH3-O-CH2-CH3
Assinale a alternativa correta.
As moléculas I e II são isômeros de posição e I e III são isômeros de função.
As moléculas I e II são isômeros de cadeia e II e III são isômeros de função.
As moléculas II e III não são isômeros.
As moléculas I e III são isômeros de cadeia, assim como as moléculas II e III.
As moléculas I e III são isômeros de posição.
A equação a seguir representa a reação entre o benzeno e o cloreto de etanoíla, onde se utilizou cloreto de alumínio como catalisador. Verifique qual o tipo de reação está sendo exemplificado:

Nitração
Acilação
Sulfonação
Cloração
Alquilação
Um determinado composto orgânico dissolvido em 50 mL de uma solução foi submetido a duas extrações líquido-líquido utilizando 10 mL de octanol. Sabe-se que a razão de distribuição para o analito é de 1/70. Considerando que, na fase aquosa, há 1,58 g do composto orgânico. Qual a massa do analito que foi extraído?
1,575 g
0,796 g
0,582 g
1,010 g
1,580 g
Um composto orgânico com características básicas pode ser removido de sua solução em um solvente orgânico, pelo tratamento com uma solução ácida. Analisando o composto abaixo, é correto afirmar que:

Possui caráter básico.
Seu respectivo sal é solúvel em água.
É um composto insolúvel em diclorometano.
Seu respectivo sal é solúvel em diclorometano.
É um composto solúvel em água.
Analisando as estruturas químicas, a seguir, explique por que o sal do ácido benzóico (benzoato de sódio) é mais solúvel em água do que o ácido benzóico.

O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.
O coeficiente de distribuição ou partição (Kd) é uma constante de equilíbrio que descreve a distribuição do soluto entre duas fases imiscíveis. Logo, para um soluto A, o coeficiente de partição, Kd, entre ligroína e água é 7,5. Que massa de A seria removida de uma solução de 10 g de A em 100 mL de água, por uma única extração com 100 mL de ligroína?
10 g
2,46 x 10-7 g
19,999 g
5 g
0,218 g
Podemos definir destilação como sendo uma operação que consiste na separação de substâncias químicas de suas eventuais misturas, baseado em suas diferenças de volatilidade. O processo de destilação é classificado como uma:
Operação unitária ou um processo de separação química, portanto ocorre reação química.
Operação unitária ou um processo de separação física, portanto não ocorre reação química.
Operação binária ocorrendo reação química.
Operação binária, não ocorrendo reação química.
Operação unitária, ou processo de separação físico-química, portanto ocorre reação química.
O controle de pulgas em animais de estimação pode ser feito utilizando-se a droga lufenurona, cuja estrutura química está representada abaixo.
 A lufenurona interfere na produção de quitina, componente que forma o exoesqueleto da pulga, levando o parasita à morte. A lufenurona possui:
A lufenurona interfere na produção de quitina, componente que forma o exoesqueleto da pulga, levando o parasita à morte. A lufenurona possui:
Um carbono assimétrico.
Seis ligações covalentes π.
A função amina.
Doze átomos de carbono com hibridização sp2.
Fórmula molecular C17H8O3N2F8Cl2.
Observe as moléculas abaixo.
I) CH3CH2CH2OH
II) CH3-CHOH-CH3
III) CH3-O-CH2-CH3
Assinale a alternativa correta.
As moléculas I e II são isômeros de posição e I e III são isômeros de função.
As moléculas I e II são isômeros de cadeia e II e III são isômeros de função.
As moléculas II e III não são isômeros.
As moléculas I e III são isômeros de cadeia, assim como as moléculas II e III.
As moléculas I e III são isômeros de posição.
A equação a seguir representa a reação entre o benzeno e o cloreto de etanoíla, onde se utilizou cloreto de alumínio como catalisador. Verifique qual o tipo de reação está sendo exemplificado:

Nitração
Acilação
Sulfonação
Cloração
Alquilação
Um determinado composto orgânico dissolvido em 50 mL de uma solução foi submetido a duas extrações líquido-líquido utilizando 10 mL de octanol. Sabe-se que a razão de distribuição para o analito é de 1/70. Considerando que, na fase aquosa, há 1,58 g do composto orgânico. Qual a massa do analito que foi extraído?
1,575 g
0,796 g
0,582 g
1,010 g
1,580 g
Um composto orgânico com características básicas pode ser removido de sua solução em um solvente orgânico, pelo tratamento com uma solução ácida. Analisando o composto abaixo, é correto afirmar que:

Possui caráter básico.
Seu respectivo sal é solúvel em água.
É um composto insolúvel em diclorometano.
Seu respectivo sal é solúvel em diclorometano.
É um composto solúvel em água.
Analisando as estruturas químicas, a seguir, explique por que o sal do ácido benzóico (benzoato de sódio) é mais solúvel em água do que o ácido benzóico.

O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.
O coeficiente de distribuição ou partição (Kd) é uma constante de equilíbrio que descreve a distribuição do soluto entre duas fases imiscíveis. Logo, para um soluto A, o coeficiente de partição, Kd, entre ligroína e água é 7,5. Que massa de A seria removida de uma solução de 10 g de A em 100 mL de água, por uma única extração com 100 mL de ligroína?
Operação unitária ou um processo de separação química, portanto ocorre reação química.
Operação unitária ou um processo de separação física, portanto não ocorre reação química.
Operação binária ocorrendo reação química.
Operação binária, não ocorrendo reação química.
Operação unitária, ou processo de separação físico-química, portanto ocorre reação química.
O controle de pulgas em animais de estimação pode ser feito utilizando-se a droga lufenurona, cuja estrutura química está representada abaixo.
 A lufenurona interfere na produção de quitina, componente que forma o exoesqueleto da pulga, levando o parasita à morte. A lufenurona possui:
A lufenurona interfere na produção de quitina, componente que forma o exoesqueleto da pulga, levando o parasita à morte. A lufenurona possui:
Um carbono assimétrico.
Seis ligações covalentes π.
A função amina.
Doze átomos de carbono com hibridização sp2.
Fórmula molecular C17H8O3N2F8Cl2.
Observe as moléculas abaixo.
I) CH3CH2CH2OH
II) CH3-CHOH-CH3
III) CH3-O-CH2-CH3
Assinale a alternativa correta.
As moléculas I e II são isômeros de posição e I e III são isômeros de função.
As moléculas I e II são isômeros de cadeia e II e III são isômeros de função.
As moléculas II e III não são isômeros.
As moléculas I e III são isômeros de cadeia, assim como as moléculas II e III.
As moléculas I e III são isômeros de posição.
A equação a seguir representa a reação entre o benzeno e o cloreto de etanoíla, onde se utilizou cloreto de alumínio como catalisador. Verifique qual o tipo de reação está sendo exemplificado:

Nitração
Acilação
Sulfonação
Cloração
Alquilação
Um determinado composto orgânico dissolvido em 50 mL de uma solução foi submetido a duas extrações líquido-líquido utilizando 10 mL de octanol. Sabe-se que a razão de distribuição para o analito é de 1/70. Considerando que, na fase aquosa, há 1,58 g do composto orgânico. Qual a massa do analito que foi extraído?
1,575 g
0,796 g
0,582 g
1,010 g
1,580 g
Um composto orgânico com características básicas pode ser removido de sua solução em um solvente orgânico, pelo tratamento com uma solução ácida. Analisando o composto abaixo, é correto afirmar que:

Possui caráter básico.
Seu respectivo sal é solúvel em água.
É um composto insolúvel em diclorometano.
Seu respectivo sal é solúvel em diclorometano.
É um composto solúvel em água.
Analisando as estruturas químicas, a seguir, explique por que o sal do ácido benzóico (benzoato de sódio) é mais solúvel em água do que o ácido benzóico.

O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.
O coeficiente de distribuição ou partição (Kd) é uma constante de equilíbrio que descreve a distribuição do soluto entre duas fases imiscíveis. Logo, para um soluto A, o coeficiente de partição, Kd, entre ligroína e água é 7,5. Que massa de A seria removida de uma solução de 10 g de A em 100 mL de água, por uma única extração com 100 mL de ligroína?
Um carbono assimétrico.
Seis ligações covalentes π.
A função amina.
Doze átomos de carbono com hibridização sp2.
Fórmula molecular C17H8O3N2F8Cl2.
Observe as moléculas abaixo.
I) CH3CH2CH2OH
II) CH3-CHOH-CH3
III) CH3-O-CH2-CH3
Assinale a alternativa correta.
As moléculas I e II são isômeros de posição e I e III são isômeros de função.
As moléculas I e II são isômeros de cadeia e II e III são isômeros de função.
As moléculas II e III não são isômeros.
As moléculas I e III são isômeros de cadeia, assim como as moléculas II e III.
As moléculas I e III são isômeros de posição.
A equação a seguir representa a reação entre o benzeno e o cloreto de etanoíla, onde se utilizou cloreto de alumínio como catalisador. Verifique qual o tipo de reação está sendo exemplificado:

Nitração
Acilação
Sulfonação
Cloração
Alquilação
Um determinado composto orgânico dissolvido em 50 mL de uma solução foi submetido a duas extrações líquido-líquido utilizando 10 mL de octanol. Sabe-se que a razão de distribuição para o analito é de 1/70. Considerando que, na fase aquosa, há 1,58 g do composto orgânico. Qual a massa do analito que foi extraído?
1,575 g
0,796 g
0,582 g
1,010 g
1,580 g
Um composto orgânico com características básicas pode ser removido de sua solução em um solvente orgânico, pelo tratamento com uma solução ácida. Analisando o composto abaixo, é correto afirmar que:

Possui caráter básico.
Seu respectivo sal é solúvel em água.
É um composto insolúvel em diclorometano.
Seu respectivo sal é solúvel em diclorometano.
É um composto solúvel em água.
Analisando as estruturas químicas, a seguir, explique por que o sal do ácido benzóico (benzoato de sódio) é mais solúvel em água do que o ácido benzóico.

O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.
O coeficiente de distribuição ou partição (Kd) é uma constante de equilíbrio que descreve a distribuição do soluto entre duas fases imiscíveis. Logo, para um soluto A, o coeficiente de partição, Kd, entre ligroína e água é 7,5. Que massa de A seria removida de uma solução de 10 g de A em 100 mL de água, por uma única extração com 100 mL de ligroína?
As moléculas I e II são isômeros de posição e I e III são isômeros de função.
As moléculas I e II são isômeros de cadeia e II e III são isômeros de função.
As moléculas II e III não são isômeros.
As moléculas I e III são isômeros de cadeia, assim como as moléculas II e III.
As moléculas I e III são isômeros de posição.
A equação a seguir representa a reação entre o benzeno e o cloreto de etanoíla, onde se utilizou cloreto de alumínio como catalisador. Verifique qual o tipo de reação está sendo exemplificado:

Nitração
Acilação
Sulfonação
Cloração
Alquilação
Um determinado composto orgânico dissolvido em 50 mL de uma solução foi submetido a duas extrações líquido-líquido utilizando 10 mL de octanol. Sabe-se que a razão de distribuição para o analito é de 1/70. Considerando que, na fase aquosa, há 1,58 g do composto orgânico. Qual a massa do analito que foi extraído?
1,575 g
0,796 g
0,582 g
1,010 g
1,580 g
Um composto orgânico com características básicas pode ser removido de sua solução em um solvente orgânico, pelo tratamento com uma solução ácida. Analisando o composto abaixo, é correto afirmar que:

Possui caráter básico.
Seu respectivo sal é solúvel em água.
É um composto insolúvel em diclorometano.
Seu respectivo sal é solúvel em diclorometano.
É um composto solúvel em água.
Analisando as estruturas químicas, a seguir, explique por que o sal do ácido benzóico (benzoato de sódio) é mais solúvel em água do que o ácido benzóico.

O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.
O coeficiente de distribuição ou partição (Kd) é uma constante de equilíbrio que descreve a distribuição do soluto entre duas fases imiscíveis. Logo, para um soluto A, o coeficiente de partição, Kd, entre ligroína e água é 7,5. Que massa de A seria removida de uma solução de 10 g de A em 100 mL de água, por uma única extração com 100 mL de ligroína?

Nitração
Acilação
Sulfonação
Cloração
Alquilação
Um determinado composto orgânico dissolvido em 50 mL de uma solução foi submetido a duas extrações líquido-líquido utilizando 10 mL de octanol. Sabe-se que a razão de distribuição para o analito é de 1/70. Considerando que, na fase aquosa, há 1,58 g do composto orgânico. Qual a massa do analito que foi extraído?
1,575 g
0,796 g
0,582 g
1,010 g
1,580 g
Um composto orgânico com características básicas pode ser removido de sua solução em um solvente orgânico, pelo tratamento com uma solução ácida. Analisando o composto abaixo, é correto afirmar que:

Possui caráter básico.
Seu respectivo sal é solúvel em água.
É um composto insolúvel em diclorometano.
Seu respectivo sal é solúvel em diclorometano.
É um composto solúvel em água.
Analisando as estruturas químicas, a seguir, explique por que o sal do ácido benzóico (benzoato de sódio) é mais solúvel em água do que o ácido benzóico.

O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.
O coeficiente de distribuição ou partição (Kd) é uma constante de equilíbrio que descreve a distribuição do soluto entre duas fases imiscíveis. Logo, para um soluto A, o coeficiente de partição, Kd, entre ligroína e água é 7,5. Que massa de A seria removida de uma solução de 10 g de A em 100 mL de água, por uma única extração com 100 mL de ligroína?
1,575 g
0,796 g
0,582 g
1,010 g
1,580 g
Um composto orgânico com características básicas pode ser removido de sua solução em um solvente orgânico, pelo tratamento com uma solução ácida. Analisando o composto abaixo, é correto afirmar que:

Possui caráter básico.
Seu respectivo sal é solúvel em água.
É um composto insolúvel em diclorometano.
Seu respectivo sal é solúvel em diclorometano.
É um composto solúvel em água.
Analisando as estruturas químicas, a seguir, explique por que o sal do ácido benzóico (benzoato de sódio) é mais solúvel em água do que o ácido benzóico.

O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.
O coeficiente de distribuição ou partição (Kd) é uma constante de equilíbrio que descreve a distribuição do soluto entre duas fases imiscíveis. Logo, para um soluto A, o coeficiente de partição, Kd, entre ligroína e água é 7,5. Que massa de A seria removida de uma solução de 10 g de A em 100 mL de água, por uma única extração com 100 mL de ligroína?

Possui caráter básico.
Seu respectivo sal é solúvel em água.
É um composto insolúvel em diclorometano.
Seu respectivo sal é solúvel em diclorometano.
É um composto solúvel em água.
Analisando as estruturas químicas, a seguir, explique por que o sal do ácido benzóico (benzoato de sódio) é mais solúvel em água do que o ácido benzóico.

O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.
O coeficiente de distribuição ou partição (Kd) é uma constante de equilíbrio que descreve a distribuição do soluto entre duas fases imiscíveis. Logo, para um soluto A, o coeficiente de partição, Kd, entre ligroína e água é 7,5. Que massa de A seria removida de uma solução de 10 g de A em 100 mL de água, por uma única extração com 100 mL de ligroína?

O benzoato de sódio, é menos solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, não é muito solúvel em água.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais polar que ácido benzóico.
O benzoato de sódio, é muito solúvel em água, pois é um composto orgânico bem mais apolar que ácido benzóico.
O ácido benzóico, é muito solúvel em água.