FÍSICO-QUÍMICA II
O peróxido de hidrogênio, mais conhecido como água oxigenada é um líquido incolor à temperatura ambiente e um poderoso oxidante. Esta substância se decompõe lentamente formando água e gás oxigênio. Sua velocidade de degradação pode ser acelerada por exposição ao sol ou com a adição de pequena quantidade de MnO2, conforme representado no esquema abaixo:
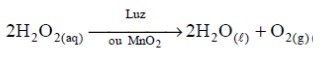
baseado nas informações dadas e nos conceitos que regem a cinética das reações é CORRETO afirmar que: