INTRODUÇÃO À QUÍMICA ORGÂNICA
A reatividade das substâncias carboniladas está relacionada com a polaridade do grupo carbonila. O oxigênio é mais eletronegativo do que o carbono. O carbono carbonílico, portanto, é um eletrófilo e por esse motivo está susceptível ao ataque de um nucleófilo. Com relação aos dois sentidos da reação, pode-se afirmar que:
Dados: MeOH (pKa = 16) ; NH3 (pKa = 9,25)
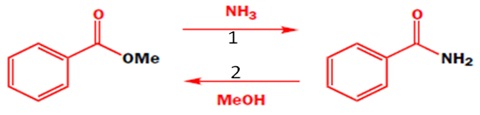
A reação no sentido 1 não ocorre, porque o NH3 é um nucleófilo fraco.
A reação no sentido 2 ocorre e o grupo NH2- será eliminado no intermediário da reação.
A reação pode ocorrer nos dois sentidos, mas preferencialmente no sentido 2.
A reação no sentido 1 ocorre, pelo fato do grupo OMe ser um melhor grupo de saída.
O grupo NH2- é uma base mais fraca que o grupo MeO-.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.
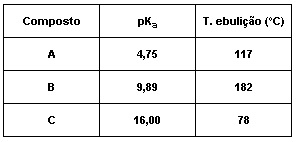 Os compostos A, B e C podem ser, respectivamente:
Os compostos A, B e C podem ser, respectivamente:
fenol - ácido acético - etanol.
etanol - fenol - ácido acético.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
ácido acético - etanol - fenol.
Considere as substâncias fenol, ácido acético, ácido benzóico e cloreto de metilamônio. Em relação a essas substâncias e a suas soluções aquosas de mesma concentração em mol.L-1, todas as alternativas estão corretas, EXCETO.
A solução de cloreto de metilamônio tem pH menor do que sete.
O fenol é uma base segundo a teoria de Arrhenius.
O pH da solução de fenol é maior do que o da solução de ácido acético.
O ácido acético reage com carbonatos produzindo gás carbônico.
O ácido benzóico é um composto aromático.
Foi desenvolvido pela Universidade de New Hampshire (EUA) um tipo de asfalto capaz de absorver até 80% da água da chuva e, assim, evitar ou amenizar as enchentes em grandes cidades. A água atravessa o asfalto, alcança o solo e escoa para os lençóis freáticos, sem se acumular. O pavimento é feito de betume, mesmo derivado do petróleo que compõe o asfalto comum, contudo, por ser menos denso, torna o asfalto permeável. Betumes são misturas de hidrocarbonetos de peso molecular elevado que podem pertencer a três grupos: alifáticos, naftênicos e aromáticos.
No que concerne ao betume e seus grupos, assinale a opção correta.
Naftênicos são cicloalcanos de fórmula geral CnH2n.
Aromáticos mononucleares com ramificações acíclicas e insaturadas são compostos de fórmula geral CnH2n – 6 (n³ 8).
Os aromáticos são ácidos carboxílicos de cadeia muito longa e insaturada.
O betume pertence ao grupo das olefinas, de cadeia exclusivamente fechada e saturada.
Alifáticos são hidrocarbonetos com átomos de carbono em cadeias exclusivamente abertas e saturadas.
Quando a água é adicionada a um alceno, nenhuma reação ocorre porque não há eletrófilo presente para dar início à reação de adição do nucleófilo ao alceno, entretanto, se um ácido for adicionado à solução, uma reação poderá acontecer porque o ácido fornece um eletrófilo à solução. Quais são as duas etapas do mecanismo para a reação de adição de água catalisada por um ácido a um alceno?
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Na primeira etapa o nucleófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o eletrófilo se adiciona ao outro carbono sp2.
Na primeira etapa o eletrófilo se adiciona ao carbono sp3 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp3.
Na primeira etapa o eletrófilo se adiciona ao carbono sp que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp.
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao menor número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Não é suficiente saber que uma substância com uma ligação dupla carbono-carbono reage com ácido bromídrico (HBr) para levar a formação de um produto com a adição de H e Br nos carbonos insaturados. É necessário entender por que a substância reage com determinadas espécies, como o HBr. Essencialmente, a química orgânica discute a interação entre átomos ou moléculas ricas em elétrons e átomos ou moléculas pobres (deficientes) de elétrons. Sobre estas espécies ricas ou pobres em elétrons, assinale a alternativa que corresponde aos itens corretos:
1 - Átomos ou moléculas ricas em elétrons são atraídos por átomos ou moléculas pobres em elétrons.
2 - Um átomo ou molécula deficiente de elétrons é chamado de eletrófilo.
3 - Um eletrófilo pode ter um átomo que aceite um par de elétrons, ou pode ter um átomo com um elétron desemparelhado, e assim, precisar de um elétron para completar seu octeto.
4 - Um átomo (ou molécula) rico em elétrons é chamado de nucleófilo, o qual possui um par de elétrons que pode compartilhar.
É correto afirmar em relação as informações acima que:
Somente 2, 3 e 4 estão corretos.
Somente 1, 3 e 4 estão corretos.
Todos os itens estão corretos.
Somente 1, 2 e 4 estão corretos.
Somente 2 e 3 estão corretos.
A reação de alcenos com haletos de hidrogênio como HCl, HI ou HBr produz um haleto orgânico. Nessas reações ocorre primeiramente a entrada do próton (H+) formando uma estrutura intermediária chama de carbocátion. A reação acontece preferencialmente no sentido de formar o carbocátion mais estável. Na reação do pent-2-eno com HBr forma-se:
2,3-dibromopentano.
Somente 2-bromopentano.
Somente 3-bromopentano.
Pent-2-eno não reage com HBr.
Uma mistura de 2-bromopentano e 3-bromopentano.
Alguns compostos em Química Orgânica possuem um tipo de isomeria denominada geométrica. Geralmente ocorre em compostos com ligação dupla ou com cadeia cíclica. Nos alcenos é preciso que os carbonos da ligação dupla possuam ligantes diferentes e o mesmo ocorre com os compostos cíclicos, é preciso que no ciclo tenha pelo menos dois carbonos com ligantes diferentes. Diante dessas informações, quais dos compostos abaixo possuem isomeria geométrica?
I. butan-2-ol
II. pent-1-eno
III. hex-2-eno
IV. 2-metil-cicloexanol
V. cicloexeno
I e IV.
II e V.
II e III.
III e IV.
I e V.
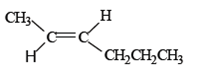
Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular e fórmulas estruturais diferentes. Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes). Dê o nome para o composto abaixo e sua respectiva isomeria geométrica:

A reação no sentido 1 não ocorre, porque o NH3 é um nucleófilo fraco.
A reação no sentido 2 ocorre e o grupo NH2- será eliminado no intermediário da reação.
A reação pode ocorrer nos dois sentidos, mas preferencialmente no sentido 2.
A reação no sentido 1 ocorre, pelo fato do grupo OMe ser um melhor grupo de saída.
O grupo NH2- é uma base mais fraca que o grupo MeO-.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.
 Os compostos A, B e C podem ser, respectivamente:
Os compostos A, B e C podem ser, respectivamente:
fenol - ácido acético - etanol.
etanol - fenol - ácido acético.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
ácido acético - etanol - fenol.
Considere as substâncias fenol, ácido acético, ácido benzóico e cloreto de metilamônio. Em relação a essas substâncias e a suas soluções aquosas de mesma concentração em mol.L-1, todas as alternativas estão corretas, EXCETO.
A solução de cloreto de metilamônio tem pH menor do que sete.
O fenol é uma base segundo a teoria de Arrhenius.
O pH da solução de fenol é maior do que o da solução de ácido acético.
O ácido acético reage com carbonatos produzindo gás carbônico.
O ácido benzóico é um composto aromático.
Foi desenvolvido pela Universidade de New Hampshire (EUA) um tipo de asfalto capaz de absorver até 80% da água da chuva e, assim, evitar ou amenizar as enchentes em grandes cidades. A água atravessa o asfalto, alcança o solo e escoa para os lençóis freáticos, sem se acumular. O pavimento é feito de betume, mesmo derivado do petróleo que compõe o asfalto comum, contudo, por ser menos denso, torna o asfalto permeável. Betumes são misturas de hidrocarbonetos de peso molecular elevado que podem pertencer a três grupos: alifáticos, naftênicos e aromáticos.
No que concerne ao betume e seus grupos, assinale a opção correta.
Naftênicos são cicloalcanos de fórmula geral CnH2n.
Aromáticos mononucleares com ramificações acíclicas e insaturadas são compostos de fórmula geral CnH2n – 6 (n³ 8).
Os aromáticos são ácidos carboxílicos de cadeia muito longa e insaturada.
O betume pertence ao grupo das olefinas, de cadeia exclusivamente fechada e saturada.
Alifáticos são hidrocarbonetos com átomos de carbono em cadeias exclusivamente abertas e saturadas.
Quando a água é adicionada a um alceno, nenhuma reação ocorre porque não há eletrófilo presente para dar início à reação de adição do nucleófilo ao alceno, entretanto, se um ácido for adicionado à solução, uma reação poderá acontecer porque o ácido fornece um eletrófilo à solução. Quais são as duas etapas do mecanismo para a reação de adição de água catalisada por um ácido a um alceno?
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Na primeira etapa o nucleófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o eletrófilo se adiciona ao outro carbono sp2.
Na primeira etapa o eletrófilo se adiciona ao carbono sp3 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp3.
Na primeira etapa o eletrófilo se adiciona ao carbono sp que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp.
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao menor número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Não é suficiente saber que uma substância com uma ligação dupla carbono-carbono reage com ácido bromídrico (HBr) para levar a formação de um produto com a adição de H e Br nos carbonos insaturados. É necessário entender por que a substância reage com determinadas espécies, como o HBr. Essencialmente, a química orgânica discute a interação entre átomos ou moléculas ricas em elétrons e átomos ou moléculas pobres (deficientes) de elétrons. Sobre estas espécies ricas ou pobres em elétrons, assinale a alternativa que corresponde aos itens corretos:
1 - Átomos ou moléculas ricas em elétrons são atraídos por átomos ou moléculas pobres em elétrons.
2 - Um átomo ou molécula deficiente de elétrons é chamado de eletrófilo.
3 - Um eletrófilo pode ter um átomo que aceite um par de elétrons, ou pode ter um átomo com um elétron desemparelhado, e assim, precisar de um elétron para completar seu octeto.
4 - Um átomo (ou molécula) rico em elétrons é chamado de nucleófilo, o qual possui um par de elétrons que pode compartilhar.
É correto afirmar em relação as informações acima que:
Somente 2, 3 e 4 estão corretos.
Somente 1, 3 e 4 estão corretos.
Todos os itens estão corretos.
Somente 1, 2 e 4 estão corretos.
Somente 2 e 3 estão corretos.
A reação de alcenos com haletos de hidrogênio como HCl, HI ou HBr produz um haleto orgânico. Nessas reações ocorre primeiramente a entrada do próton (H+) formando uma estrutura intermediária chama de carbocátion. A reação acontece preferencialmente no sentido de formar o carbocátion mais estável. Na reação do pent-2-eno com HBr forma-se:
2,3-dibromopentano.
Somente 2-bromopentano.
Somente 3-bromopentano.
Pent-2-eno não reage com HBr.
Uma mistura de 2-bromopentano e 3-bromopentano.
Alguns compostos em Química Orgânica possuem um tipo de isomeria denominada geométrica. Geralmente ocorre em compostos com ligação dupla ou com cadeia cíclica. Nos alcenos é preciso que os carbonos da ligação dupla possuam ligantes diferentes e o mesmo ocorre com os compostos cíclicos, é preciso que no ciclo tenha pelo menos dois carbonos com ligantes diferentes. Diante dessas informações, quais dos compostos abaixo possuem isomeria geométrica?
I. butan-2-ol
II. pent-1-eno
III. hex-2-eno
IV. 2-metil-cicloexanol
V. cicloexeno
I e IV.
II e V.
II e III.
III e IV.
I e V.
Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular e fórmulas estruturais diferentes. Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes). Dê o nome para o composto abaixo e sua respectiva isomeria geométrica:

fenol - ácido acético - etanol.
etanol - fenol - ácido acético.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
ácido acético - etanol - fenol.
Considere as substâncias fenol, ácido acético, ácido benzóico e cloreto de metilamônio. Em relação a essas substâncias e a suas soluções aquosas de mesma concentração em mol.L-1, todas as alternativas estão corretas, EXCETO.
A solução de cloreto de metilamônio tem pH menor do que sete.
O fenol é uma base segundo a teoria de Arrhenius.
O pH da solução de fenol é maior do que o da solução de ácido acético.
O ácido acético reage com carbonatos produzindo gás carbônico.
O ácido benzóico é um composto aromático.
Foi desenvolvido pela Universidade de New Hampshire (EUA) um tipo de asfalto capaz de absorver até 80% da água da chuva e, assim, evitar ou amenizar as enchentes em grandes cidades. A água atravessa o asfalto, alcança o solo e escoa para os lençóis freáticos, sem se acumular. O pavimento é feito de betume, mesmo derivado do petróleo que compõe o asfalto comum, contudo, por ser menos denso, torna o asfalto permeável. Betumes são misturas de hidrocarbonetos de peso molecular elevado que podem pertencer a três grupos: alifáticos, naftênicos e aromáticos.
No que concerne ao betume e seus grupos, assinale a opção correta.
Naftênicos são cicloalcanos de fórmula geral CnH2n.
Aromáticos mononucleares com ramificações acíclicas e insaturadas são compostos de fórmula geral CnH2n – 6 (n³ 8).
Os aromáticos são ácidos carboxílicos de cadeia muito longa e insaturada.
O betume pertence ao grupo das olefinas, de cadeia exclusivamente fechada e saturada.
Alifáticos são hidrocarbonetos com átomos de carbono em cadeias exclusivamente abertas e saturadas.
Quando a água é adicionada a um alceno, nenhuma reação ocorre porque não há eletrófilo presente para dar início à reação de adição do nucleófilo ao alceno, entretanto, se um ácido for adicionado à solução, uma reação poderá acontecer porque o ácido fornece um eletrófilo à solução. Quais são as duas etapas do mecanismo para a reação de adição de água catalisada por um ácido a um alceno?
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Na primeira etapa o nucleófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o eletrófilo se adiciona ao outro carbono sp2.
Na primeira etapa o eletrófilo se adiciona ao carbono sp3 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp3.
Na primeira etapa o eletrófilo se adiciona ao carbono sp que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp.
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao menor número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Não é suficiente saber que uma substância com uma ligação dupla carbono-carbono reage com ácido bromídrico (HBr) para levar a formação de um produto com a adição de H e Br nos carbonos insaturados. É necessário entender por que a substância reage com determinadas espécies, como o HBr. Essencialmente, a química orgânica discute a interação entre átomos ou moléculas ricas em elétrons e átomos ou moléculas pobres (deficientes) de elétrons. Sobre estas espécies ricas ou pobres em elétrons, assinale a alternativa que corresponde aos itens corretos:
1 - Átomos ou moléculas ricas em elétrons são atraídos por átomos ou moléculas pobres em elétrons.
2 - Um átomo ou molécula deficiente de elétrons é chamado de eletrófilo.
3 - Um eletrófilo pode ter um átomo que aceite um par de elétrons, ou pode ter um átomo com um elétron desemparelhado, e assim, precisar de um elétron para completar seu octeto.
4 - Um átomo (ou molécula) rico em elétrons é chamado de nucleófilo, o qual possui um par de elétrons que pode compartilhar.
É correto afirmar em relação as informações acima que:
Somente 2, 3 e 4 estão corretos.
Somente 1, 3 e 4 estão corretos.
Todos os itens estão corretos.
Somente 1, 2 e 4 estão corretos.
Somente 2 e 3 estão corretos.
A reação de alcenos com haletos de hidrogênio como HCl, HI ou HBr produz um haleto orgânico. Nessas reações ocorre primeiramente a entrada do próton (H+) formando uma estrutura intermediária chama de carbocátion. A reação acontece preferencialmente no sentido de formar o carbocátion mais estável. Na reação do pent-2-eno com HBr forma-se:
2,3-dibromopentano.
Somente 2-bromopentano.
Somente 3-bromopentano.
Pent-2-eno não reage com HBr.
Uma mistura de 2-bromopentano e 3-bromopentano.
Alguns compostos em Química Orgânica possuem um tipo de isomeria denominada geométrica. Geralmente ocorre em compostos com ligação dupla ou com cadeia cíclica. Nos alcenos é preciso que os carbonos da ligação dupla possuam ligantes diferentes e o mesmo ocorre com os compostos cíclicos, é preciso que no ciclo tenha pelo menos dois carbonos com ligantes diferentes. Diante dessas informações, quais dos compostos abaixo possuem isomeria geométrica?
I. butan-2-ol
II. pent-1-eno
III. hex-2-eno
IV. 2-metil-cicloexanol
V. cicloexeno
I e IV.
II e V.
II e III.
III e IV.
I e V.
Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular e fórmulas estruturais diferentes. Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes). Dê o nome para o composto abaixo e sua respectiva isomeria geométrica:

A solução de cloreto de metilamônio tem pH menor do que sete.
O fenol é uma base segundo a teoria de Arrhenius.
O pH da solução de fenol é maior do que o da solução de ácido acético.
O ácido acético reage com carbonatos produzindo gás carbônico.
O ácido benzóico é um composto aromático.
Foi desenvolvido pela Universidade de New Hampshire (EUA) um tipo de asfalto capaz de absorver até 80% da água da chuva e, assim, evitar ou amenizar as enchentes em grandes cidades. A água atravessa o asfalto, alcança o solo e escoa para os lençóis freáticos, sem se acumular. O pavimento é feito de betume, mesmo derivado do petróleo que compõe o asfalto comum, contudo, por ser menos denso, torna o asfalto permeável. Betumes são misturas de hidrocarbonetos de peso molecular elevado que podem pertencer a três grupos: alifáticos, naftênicos e aromáticos.
No que concerne ao betume e seus grupos, assinale a opção correta.
Naftênicos são cicloalcanos de fórmula geral CnH2n.
Aromáticos mononucleares com ramificações acíclicas e insaturadas são compostos de fórmula geral CnH2n – 6 (n³ 8).
Os aromáticos são ácidos carboxílicos de cadeia muito longa e insaturada.
O betume pertence ao grupo das olefinas, de cadeia exclusivamente fechada e saturada.
Alifáticos são hidrocarbonetos com átomos de carbono em cadeias exclusivamente abertas e saturadas.
Quando a água é adicionada a um alceno, nenhuma reação ocorre porque não há eletrófilo presente para dar início à reação de adição do nucleófilo ao alceno, entretanto, se um ácido for adicionado à solução, uma reação poderá acontecer porque o ácido fornece um eletrófilo à solução. Quais são as duas etapas do mecanismo para a reação de adição de água catalisada por um ácido a um alceno?
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Na primeira etapa o nucleófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o eletrófilo se adiciona ao outro carbono sp2.
Na primeira etapa o eletrófilo se adiciona ao carbono sp3 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp3.
Na primeira etapa o eletrófilo se adiciona ao carbono sp que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp.
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao menor número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Não é suficiente saber que uma substância com uma ligação dupla carbono-carbono reage com ácido bromídrico (HBr) para levar a formação de um produto com a adição de H e Br nos carbonos insaturados. É necessário entender por que a substância reage com determinadas espécies, como o HBr. Essencialmente, a química orgânica discute a interação entre átomos ou moléculas ricas em elétrons e átomos ou moléculas pobres (deficientes) de elétrons. Sobre estas espécies ricas ou pobres em elétrons, assinale a alternativa que corresponde aos itens corretos:
1 - Átomos ou moléculas ricas em elétrons são atraídos por átomos ou moléculas pobres em elétrons.
2 - Um átomo ou molécula deficiente de elétrons é chamado de eletrófilo.
3 - Um eletrófilo pode ter um átomo que aceite um par de elétrons, ou pode ter um átomo com um elétron desemparelhado, e assim, precisar de um elétron para completar seu octeto.
4 - Um átomo (ou molécula) rico em elétrons é chamado de nucleófilo, o qual possui um par de elétrons que pode compartilhar.
É correto afirmar em relação as informações acima que:
Somente 2, 3 e 4 estão corretos.
Somente 1, 3 e 4 estão corretos.
Todos os itens estão corretos.
Somente 1, 2 e 4 estão corretos.
Somente 2 e 3 estão corretos.
A reação de alcenos com haletos de hidrogênio como HCl, HI ou HBr produz um haleto orgânico. Nessas reações ocorre primeiramente a entrada do próton (H+) formando uma estrutura intermediária chama de carbocátion. A reação acontece preferencialmente no sentido de formar o carbocátion mais estável. Na reação do pent-2-eno com HBr forma-se:
2,3-dibromopentano.
Somente 2-bromopentano.
Somente 3-bromopentano.
Pent-2-eno não reage com HBr.
Uma mistura de 2-bromopentano e 3-bromopentano.
Alguns compostos em Química Orgânica possuem um tipo de isomeria denominada geométrica. Geralmente ocorre em compostos com ligação dupla ou com cadeia cíclica. Nos alcenos é preciso que os carbonos da ligação dupla possuam ligantes diferentes e o mesmo ocorre com os compostos cíclicos, é preciso que no ciclo tenha pelo menos dois carbonos com ligantes diferentes. Diante dessas informações, quais dos compostos abaixo possuem isomeria geométrica?
I. butan-2-ol
II. pent-1-eno
III. hex-2-eno
IV. 2-metil-cicloexanol
V. cicloexeno
I e IV.
II e V.
II e III.
III e IV.
I e V.
Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular e fórmulas estruturais diferentes. Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes). Dê o nome para o composto abaixo e sua respectiva isomeria geométrica:

Naftênicos são cicloalcanos de fórmula geral CnH2n.
Aromáticos mononucleares com ramificações acíclicas e insaturadas são compostos de fórmula geral CnH2n – 6 (n³ 8).
Os aromáticos são ácidos carboxílicos de cadeia muito longa e insaturada.
O betume pertence ao grupo das olefinas, de cadeia exclusivamente fechada e saturada.
Alifáticos são hidrocarbonetos com átomos de carbono em cadeias exclusivamente abertas e saturadas.
Quando a água é adicionada a um alceno, nenhuma reação ocorre porque não há eletrófilo presente para dar início à reação de adição do nucleófilo ao alceno, entretanto, se um ácido for adicionado à solução, uma reação poderá acontecer porque o ácido fornece um eletrófilo à solução. Quais são as duas etapas do mecanismo para a reação de adição de água catalisada por um ácido a um alceno?
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Na primeira etapa o nucleófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o eletrófilo se adiciona ao outro carbono sp2.
Na primeira etapa o eletrófilo se adiciona ao carbono sp3 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp3.
Na primeira etapa o eletrófilo se adiciona ao carbono sp que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp.
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao menor número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Não é suficiente saber que uma substância com uma ligação dupla carbono-carbono reage com ácido bromídrico (HBr) para levar a formação de um produto com a adição de H e Br nos carbonos insaturados. É necessário entender por que a substância reage com determinadas espécies, como o HBr. Essencialmente, a química orgânica discute a interação entre átomos ou moléculas ricas em elétrons e átomos ou moléculas pobres (deficientes) de elétrons. Sobre estas espécies ricas ou pobres em elétrons, assinale a alternativa que corresponde aos itens corretos:
1 - Átomos ou moléculas ricas em elétrons são atraídos por átomos ou moléculas pobres em elétrons.
2 - Um átomo ou molécula deficiente de elétrons é chamado de eletrófilo.
3 - Um eletrófilo pode ter um átomo que aceite um par de elétrons, ou pode ter um átomo com um elétron desemparelhado, e assim, precisar de um elétron para completar seu octeto.
4 - Um átomo (ou molécula) rico em elétrons é chamado de nucleófilo, o qual possui um par de elétrons que pode compartilhar.
É correto afirmar em relação as informações acima que:
Somente 2, 3 e 4 estão corretos.
Somente 1, 3 e 4 estão corretos.
Todos os itens estão corretos.
Somente 1, 2 e 4 estão corretos.
Somente 2 e 3 estão corretos.
A reação de alcenos com haletos de hidrogênio como HCl, HI ou HBr produz um haleto orgânico. Nessas reações ocorre primeiramente a entrada do próton (H+) formando uma estrutura intermediária chama de carbocátion. A reação acontece preferencialmente no sentido de formar o carbocátion mais estável. Na reação do pent-2-eno com HBr forma-se:
2,3-dibromopentano.
Somente 2-bromopentano.
Somente 3-bromopentano.
Pent-2-eno não reage com HBr.
Uma mistura de 2-bromopentano e 3-bromopentano.
Alguns compostos em Química Orgânica possuem um tipo de isomeria denominada geométrica. Geralmente ocorre em compostos com ligação dupla ou com cadeia cíclica. Nos alcenos é preciso que os carbonos da ligação dupla possuam ligantes diferentes e o mesmo ocorre com os compostos cíclicos, é preciso que no ciclo tenha pelo menos dois carbonos com ligantes diferentes. Diante dessas informações, quais dos compostos abaixo possuem isomeria geométrica?
I. butan-2-ol
II. pent-1-eno
III. hex-2-eno
IV. 2-metil-cicloexanol
V. cicloexeno
I e IV.
II e V.
II e III.
III e IV.
I e V.
Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular e fórmulas estruturais diferentes. Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes). Dê o nome para o composto abaixo e sua respectiva isomeria geométrica:

Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Na primeira etapa o nucleófilo se adiciona ao carbono sp2 que está ligado ao maior número de hidrogênios e na segunda etapa o eletrófilo se adiciona ao outro carbono sp2.
Na primeira etapa o eletrófilo se adiciona ao carbono sp3 que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp3.
Na primeira etapa o eletrófilo se adiciona ao carbono sp que está ligado ao maior número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp.
Na primeira etapa o eletrófilo se adiciona ao carbono sp2 que está ligado ao menor número de hidrogênios e na segunda etapa o nucleófilo se adiciona ao outro carbono sp2.
Não é suficiente saber que uma substância com uma ligação dupla carbono-carbono reage com ácido bromídrico (HBr) para levar a formação de um produto com a adição de H e Br nos carbonos insaturados. É necessário entender por que a substância reage com determinadas espécies, como o HBr. Essencialmente, a química orgânica discute a interação entre átomos ou moléculas ricas em elétrons e átomos ou moléculas pobres (deficientes) de elétrons. Sobre estas espécies ricas ou pobres em elétrons, assinale a alternativa que corresponde aos itens corretos:
1 - Átomos ou moléculas ricas em elétrons são atraídos por átomos ou moléculas pobres em elétrons.
2 - Um átomo ou molécula deficiente de elétrons é chamado de eletrófilo.
3 - Um eletrófilo pode ter um átomo que aceite um par de elétrons, ou pode ter um átomo com um elétron desemparelhado, e assim, precisar de um elétron para completar seu octeto.
4 - Um átomo (ou molécula) rico em elétrons é chamado de nucleófilo, o qual possui um par de elétrons que pode compartilhar.
É correto afirmar em relação as informações acima que:
Somente 2, 3 e 4 estão corretos.
Somente 1, 3 e 4 estão corretos.
Todos os itens estão corretos.
Somente 1, 2 e 4 estão corretos.
Somente 2 e 3 estão corretos.
A reação de alcenos com haletos de hidrogênio como HCl, HI ou HBr produz um haleto orgânico. Nessas reações ocorre primeiramente a entrada do próton (H+) formando uma estrutura intermediária chama de carbocátion. A reação acontece preferencialmente no sentido de formar o carbocátion mais estável. Na reação do pent-2-eno com HBr forma-se:
2,3-dibromopentano.
Somente 2-bromopentano.
Somente 3-bromopentano.
Pent-2-eno não reage com HBr.
Uma mistura de 2-bromopentano e 3-bromopentano.
Alguns compostos em Química Orgânica possuem um tipo de isomeria denominada geométrica. Geralmente ocorre em compostos com ligação dupla ou com cadeia cíclica. Nos alcenos é preciso que os carbonos da ligação dupla possuam ligantes diferentes e o mesmo ocorre com os compostos cíclicos, é preciso que no ciclo tenha pelo menos dois carbonos com ligantes diferentes. Diante dessas informações, quais dos compostos abaixo possuem isomeria geométrica?
I. butan-2-ol
II. pent-1-eno
III. hex-2-eno
IV. 2-metil-cicloexanol
V. cicloexeno
I e IV.
II e V.
II e III.
III e IV.
I e V.
Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular e fórmulas estruturais diferentes. Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes). Dê o nome para o composto abaixo e sua respectiva isomeria geométrica:

Somente 2, 3 e 4 estão corretos.
Somente 1, 3 e 4 estão corretos.
Todos os itens estão corretos.
Somente 1, 2 e 4 estão corretos.
Somente 2 e 3 estão corretos.
A reação de alcenos com haletos de hidrogênio como HCl, HI ou HBr produz um haleto orgânico. Nessas reações ocorre primeiramente a entrada do próton (H+) formando uma estrutura intermediária chama de carbocátion. A reação acontece preferencialmente no sentido de formar o carbocátion mais estável. Na reação do pent-2-eno com HBr forma-se:
2,3-dibromopentano.
Somente 2-bromopentano.
Somente 3-bromopentano.
Pent-2-eno não reage com HBr.
Uma mistura de 2-bromopentano e 3-bromopentano.
Alguns compostos em Química Orgânica possuem um tipo de isomeria denominada geométrica. Geralmente ocorre em compostos com ligação dupla ou com cadeia cíclica. Nos alcenos é preciso que os carbonos da ligação dupla possuam ligantes diferentes e o mesmo ocorre com os compostos cíclicos, é preciso que no ciclo tenha pelo menos dois carbonos com ligantes diferentes. Diante dessas informações, quais dos compostos abaixo possuem isomeria geométrica?
I. butan-2-ol
II. pent-1-eno
III. hex-2-eno
IV. 2-metil-cicloexanol
V. cicloexeno
I e IV.
II e V.
II e III.
III e IV.
I e V.
Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular e fórmulas estruturais diferentes. Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes). Dê o nome para o composto abaixo e sua respectiva isomeria geométrica:

2,3-dibromopentano.
Somente 2-bromopentano.
Somente 3-bromopentano.
Pent-2-eno não reage com HBr.
Uma mistura de 2-bromopentano e 3-bromopentano.
Alguns compostos em Química Orgânica possuem um tipo de isomeria denominada geométrica. Geralmente ocorre em compostos com ligação dupla ou com cadeia cíclica. Nos alcenos é preciso que os carbonos da ligação dupla possuam ligantes diferentes e o mesmo ocorre com os compostos cíclicos, é preciso que no ciclo tenha pelo menos dois carbonos com ligantes diferentes. Diante dessas informações, quais dos compostos abaixo possuem isomeria geométrica?
I. butan-2-ol
II. pent-1-eno
III. hex-2-eno
IV. 2-metil-cicloexanol
V. cicloexeno
I e IV.
II e V.
II e III.
III e IV.
I e V.
Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular e fórmulas estruturais diferentes. Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes). Dê o nome para o composto abaixo e sua respectiva isomeria geométrica:

I e IV.
II e V.
II e III.
III e IV.
I e V.
Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular e fórmulas estruturais diferentes. Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes). Dê o nome para o composto abaixo e sua respectiva isomeria geométrica:


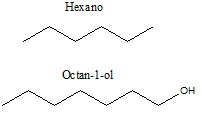 Com relação a solubilidade destes compostos em água, é correto afirmar que:
Com relação a solubilidade destes compostos em água, é correto afirmar que: